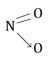
Bài 3.16 trang 21 Sách bài tập (SBT) Hóa học 10 Nâng caoGiải bài 3.16 trang 21 Sách bài tập (SBT) Hóa học 10 Nâng cao. Thế nào là liên kết cho – nhận. Hãy xác định kiểu liên kết có trong phân tử NO2. Bài 3.16 trang 21 SBT Hóa học 10 Nâng cao Thế nào là liên kết cho – nhận. Hãy xác định kiểu liên kết có trong phân tử NO2. Giải Liên kết cho – nhận là liên kết CHT phân cực do hai nguyên tử dùng chung một cặp electron thuộc về một nguyên tử trước khi tham gia tạo liên kết. Xét phân tử NO2: Trong phân tử NO (xem bài 3.14), nguyên tử oxi có đủ 8 electron ở lớp ngoài cùng và thỏa mãn quy tắc bát tử. Nguyên nhân nitơ chỉ còn 1 electron độc thân không đủ để ghép đôi với hai electron độc thân của một nguyên tử oxi thứ hai. Liên kết cộng hóa trị giữa nguyên tử nitơ và nguyên tử oxi thứ hai sẽ được thực hiện bằng sự cho – nhận cặp electron của nguyên tử nitơ. Như vậy nguyên tử oxi thứ hai cũng có 8 electron. Nguyên tử nitơ vẫn chỉ có 7 electron. Như vậy, trong phân tử NO2 có 3 liên kết cộng hóa trị. Công thức cấu tạo của NO2:
Sachbaitap.com
Xem thêm tại đây:
Bài 17: Liên kết cộng hóa trị
|
-

Bài 3.17 trang 22 Sách bài tập (SBT) Hóa học 10 Nâng cao
Giải bài 3.17 trang 22 Sách bài tập (SBT) Hóa học 10 Nâng cao. Tại sao góc liên kết trong phân tử CH4 có giá trị bằng...
-

Bài 3.18 trang 22 Sách bài tập (SBT) Hóa học 10 Nâng cao
Giải bài 3.18 trang 22 Sách bài tập (SBT) Hóa học 10 Nâng cao. Nêu thí dụ.
-

Bài 3.19 trang 22 Sách bài tập (SBT) Hóa học 10 Nâng cao
Giải bài 3.19 trang 22 Sách bài tập (SBT) Hóa học 10 Nâng cao. Hãy giải thích nguyên nhân làm cho các phân tử BeH2 có dạng thẳng.
-

Bài 3.20, 3.21, 3.22 trang 22 Sách bài tập (SBT) Hóa học 10 Nâng cao
Giải bài 3.20, 3.21, 3.22 trang 22 Sách bài tập (SBT) Hóa học 10 Nâng cao. Hãy chọn đáp án đúng.

 Tải ngay
Tải ngay