Bài 3.21 trang 28 Sách bài tập (SBT) Hóa học 11 Nâng caoGiải bài 3.21 trang 28 Sách bài tập (SBT) Hóa học 11 Nâng cao. Thành phần hóa học của một loại thủy tinh được biểu hiện bằng công thức Thành phần hóa học của một loại thủy tinh được biểu hiện bằng công thức \(N{a_2}O.CaO.6Si{O_2}\). Hãy tính khối lượng \(N{a_2}C{O_3},CaC{O_3}\,và\,Si{O_2}\) cần dùng để có thể sản xuất được 23,9 tấn thủy tinh trên. Coi hiệu suất của quá trình là 100 %. Giải: Khối lượng 1 mol thủy tinh \(N{a_2}O.CaO.6Si{O_2}\) là 478 g. Để có 23,9 g (0,05 mol) thủy tinh cần 0,05 mol Na2CO3 0,05 mol \(CaC{O_3}\,0,3\,mol\,Si{O_2}\) Từ đó tính được 5,3 tấn Na2CO3, 5 tấn CaCO3 và 18 tấn SiO2. Sachbaitap.com
Xem thêm tại đây:
Bài 23: Công nghiệp silicat
|
-

Bài 3.22 trang 29 Sách bài tập (SBT) Hóa học 11 Nâng cao
Giải bài 3.22 trang 29 Sách bài tập (SBT) Hóa học 11 Nâng cao. Khi nung 30 g SiO2 với 30 g Mg trong điều kiện không có không khí, thu được chất rắn A.
-

Bài 3.23 trang 29 Sách bài tập (SBT) Hóa học 11 Nâng cao
Giải bài 3.23 trang 29 Sách bài tập (SBT) Hóa học 11 Nâng cao. Nguyên tử của hai nguyên tố cacbon và silic đều có
-

Bài 3.24 trang 29 Sách bài tập (SBT) Hóa học 11 Nâng cao
Giải bài 3.24 trang 29 Sách bài tập (SBT) Hóa học 11 Nâng cao. Cacbon và silic cùng phản ứng với tất cả các chất trong nhóm nào sau đây ?
-
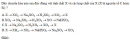
Bài 3.25 trang 29 Sách bài tập (SBT) Hóa học 11 Nâng cao
Giải bài 3.25 trang 29 Sách bài tập (SBT) Hóa học 11 Nâng cao. Dãy chuyển hóa nào sau đây đúng với tính chất X và các hợp chất của X (X là nguyên tố C hoặc Si) ?

 Tải ngay
Tải ngay