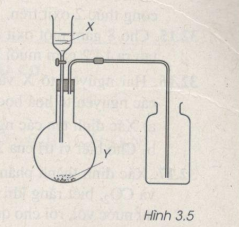
Bài 32.7 Trang 41 Sách bài tập (SBT) Hóa học 9Hình vẽ 3.5 là thiết bị điều chế khí clo trong phòng thí nghiệm 32.7. Hình vẽ 3.5 là thiết bị điều chế khí clo trong phòng thí nghiệm.
a) X và Y là những chất nào trong số các chất sau ? X : H2O, dd HCl, dd H2SO4, dd NaOH, dd NaCl. Y : NaCl, CaCO3, MnO2, CuCl2, Na2S04, KMn04. Viết phương trình hoá học điều chế khí clo từ những chất đã chọn ở trên. Trả lời a) X là : dd HC Y là : MnO2, KMnO4 b) Phương trình hoá học của phản ứng điều chế clo. \(Mn{O_2} + 4HCl \to MnC{l_2} + 2{H_2}O + C{l_2} \uparrow \) \(2KMn{O_4} + 16HCl \to 2KCl + 2MnC{l_2} + 5C{l_2} \uparrow + 8{H_2}O\)
Xem lời giải SGK - Hóa 9 - Xem ngay >> Học trực tuyến lớp 9 và Lộ trình UP10 trên Tuyensinh247.com . Học online tại nhà cũng giáo viên giỏi từ trường TOP đầu cả nước. Lộ trình học tập 3 giai đoạn: Học nền tảng lớp 9, Ôn thi vào lớp 10, Luyện Đề. Bứt phá điểm lớp 9, thi vào lớp 10 kết quả cao. Hoàn trả học phí nếu học không hiệu quả. Phụ huynh và học sinh tham khảo chi tiết khoá học tại: Link
|
-
Bài 32.8 Trang 41 Sách bài tập (SBT) Hóa học 9
Một nguyên tố X tạo được các hợp chất sau : XH3, X205. Trong bảng tuần hoàn các nguyên tố hoá học, nguyên tố X cùng nhóm với
-

Bài 32.9 Trang 41 Sách bài tập (SBT) Hóa học 9
Cho kim loại Al có dư vào 400 ml dung dịch HCl 1M. Dẫn khí tạo ra qua ống đựng CuO dư, nung nóng thì thu được 11,52 gam Cu. Tính hiệu suất của quá trình phản ứng.
-
Bài 32.10 Trang 41 Sách Bài tập (SBT) Hóa học 9
Nung hỗn hợp CaC03 và MgC03 thu được 76 gam hai oxit và 33,6 lít CO2 (đktc). Tính khối lượng của hỗn hợp ban đầu.
-
Bài 32.11* Trang 41 Sách bài tập (SBT) Hóa học 9
Có hai lá kẽm khối lượng như nhau. Một lá cho vào dung dịch đồng(II) nitrat, lá kia cho vào dung dịch chì(II) nitrat. Sau cùng một thời gian phản ứng, khối lượng lá kẽm thứ nhất giảm 0,05 gam.

 Tải ngay
Tải ngay