Bài 5.17 trang 43 Sách bài tập (SBT) Hóa học 11 Nâng caoGiải bài 5.17 trang 43 Sách bài tập (SBT) Hóa học 11 Nâng cao. Để đốt cháy một lượng hidrocacbon X cần 7,68 g oxi. Sản phẩm cháy được dẫn qua bình (1) Để đốt cháy một lượng hidrocacbon X cần 7,68 g oxi. Sản phẩm cháy được dẫn qua bình (1) đựng \({H_2}S{O_4}\) đặc, sau đó qua bình (2) đựng \(Ca{\left( {OH} \right)_2}\) dư thấy bình (1) tăng 4,32 g, bình (2) có m gam kết tủa. Xác định công thức phân tử của X. Tính khối lượng kết tủa tạo thành. Giải: CTPT của X : \({C_x}{H_y}\) \({C_x}{H_y} + (x + {y \over 4}){O_2} \to xC{O_2}+ {y \over 2}{H_2}O\) \({m_{{H_2}O}} = 4,32\,(g)\) \({n_{{H_2}O}} = {{4,32} \over {18}} = 0,24\,(mol);\) \({n_H} = 0,48\,(mol)\) Khối lượng oxi chứa trong \({H_2}O\) là 0,24 . 16= 3,84 (g) Khối lượng oxi trong \(C{O_2}\) : 7,68 – 3,84 = 3,84 (g) Khối lượng \(C{O_2}\) tạo ra \(\eqalign{ & {m_{C{O_2}}} = {{3,84.44} \over {32}} = 5,28\,(g) \cr & {n_{C{O_2}}} = 0,12\,(mol)\,\,;\,{n_C} = 0,12\,(mol) \cr} \) Ta thấy \({n_C}:{n_H} = 0,12:0,48 = 1:4\) Vậy X có công thức đông giản nhất \(C{H_4}\) CTPT của X có dạng (\(C{H_4}\)). Biện luận ta được n=1 là thõa mãn X là \(C{H_4}\) Khí \(C{O_2}\) tác dụng với dung dịch \(Ca{(OH)_2}\,\) dư \(\eqalign{ & C{O_2} + Ca{(OH)_2} \to CaC{O_3} \downarrow + {H_2}O \cr & {n_{CaC{O_3}}} = {n_{C{O_2}}} = 0,12\,(mol) \cr} \) Khối lượng kết tủa m =12 (g). Sachbaitap.com
Xem thêm tại đây:
Bài 35. An kan : Tính chất hóa học, điều chế và ứng dụng
|
-
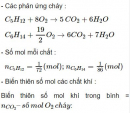
Bài 5.18 trang 44 Sách bài tập (SBT) Hóa học 11 Nâng cao
Giải bài 5.18 trang 44 Sách bài tập (SBT) Hóa học 11 Nâng cao. Tiến hành thí nghiệm ; Hai bình úp ngược (a) và (b) có thể tích bằng nhau chứa không khí dư với một bát sứ nhỏ đứng 1g ...
-

Bài 5.19 trang 44 Sách bài tập (SBT) Hóa học 11 Nâng cao
Giải bài 5.19 trang 44 Sách bài tập (SBT) Hóa học 11 Nâng cao. Cho butan tác ụng với clo khi có chiếu sáng thu được hỗn hợp hai sản phẩm đông phân của nhau chứa một nguyển tử clo trong phân tử.
-

Bài 5.20 trang 44 Sách bài tập (SBT) Hóa học 11 Nâng cao
Giải bài 5.20 trang 44 Sách bài tập (SBT) Hóa học 11 Nâng cao. Theo chiều tăng số nguyên tử cacbon trong dãy đồng đẳng, phần trăm khối lượng của nguyên tố cacbon trong phân tử xicloankan
-

Bài 5.21 trang 44 Sách bài tập (SBT) Hóa học 11 Nâng cao
Giải bài 5.21 trang 44 Sách bài tập (SBT) Hóa học 11 Nâng cao. Có hai bình đựng dung dịch brom. Sục khí propan vào bình thứ nhất có thể thu được mấy dẫn xuất monoclo ?

 Tải ngay
Tải ngay