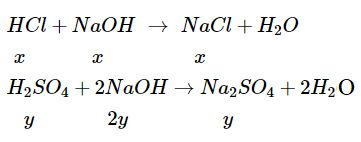Bài 5.66 trang 47 Sách bài tập (SBT) Hóa học 10 Nâng caoGiải bài 5.66 trang 47 Sách bài tập (SBT) Hóa học 10 Nâng cao. Cô cạn dung dịch sau khi trung hòa, thu được 3,76 g hỗn hợp muối khan. Xác định nồng độ mol/l của từng axit trong dung dịch A. Bài 5.66 trang 47 SBT Hóa học 10 Nâng cao Dung dịch A có chứa đồng thời hai axit: HCl và H2SO4. Để trung hòa 40 ml A cần dùng vừa hết 60 ml dung dịch NaOH 1M. Cô cạn dung dịch sau khi trung hòa, thu được 3,76 g hỗn hợp muối khan. Xác định nồng độ mol/l của từng axit trong dung dịch A. Giải Giả sử trong 40 ml dung dịch A có x mol HCl và y mol H2SO4
Số mol NaOH: \(x + 2y = {{1 \times 60} \over {1000}} = 0,06\,\,\,\,\left( 1 \right)\) Khối lượng 2 muối: \(58,5x + 142y = 3,76\,\,\,\left( 2 \right)\) Từ (1) và (2) tìm được x = 0,04; y = 0,01. Nồng độ HCl \( = {{0,04} \over {0,04}} = 1\,\left( {mol/l} \right);\,\) \({H_2}S{O_4} = {{0,01} \over {0,04}} = 0,25\,\,\left( {mol/l} \right)\) Sachbaitap.com
Xem thêm tại đây:
Bài 37: Luyện tập chương 5
|

 Tải ngay
Tải ngay