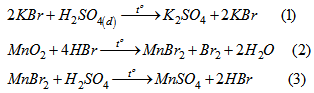Bài 5.72 trang 56 Sách bài tập (SBT) Hóa học 10Có 4 lọ không có nhãn đựng riêng biệt các muối : KF, KCl, KBr, KI. Hãy cho biết : a)Cách phân biệt muối đựng trong mỗi lọ bằng phương pháp hoá học. b)Từ những muối đã cho điều chế các halogen tương ứng và các hiđro halogenua tương ứng. Có 4 lọ không có nhãn đựng riêng biệt các muối : KF, KCl, KBr, KI. Hãy cho biết : a)Cách phân biệt muối đựng trong mỗi lọ bằng phương pháp hoá học. b)Từ những muối đã cho điều chế các halogen tương ứng và các hiđro halogenua tương ứng. Lời giải: a) Lấy một ít muối trong mỗi lọ đem hoà tan vào nước được các dung dịch riêng biệt. Dung dịch nào tác dụng được với \(Br_2\) hoặc nước brom tạo ra tinh thể có màu đen tím, đó là dung dịch KI. \(Br_2 + 2KI → 2KBr + I_2\) Những dung dịch còn lại, dung dịch nào tác dụng được với \(Cl_2\) tạo ra dung dịch có màu vàng nâu (màu của\( Br_2\) tan trong nước), đó là dung dịch KBr. \(Cl_2 + 2KBr → 2KC1 + Br_2\) Hai dung dịch còn lại là KF và KC1 : cho tác dụng với dung dịch AgNO_3, dung dịch nào tạo kết tủa trắng, đó là dung dịch KC1. \(KCl + AgNO_3 → AgCl↓ + KNO_3\) Dung dịch còn lại là KF. b) Điều chế halogen tương ứng từ muối đã cho : Điều chế \(F_2\) : Điện phân mưối KF tan trong chất lỏng HF khan thu được \(F_2\) ở anôt. Điều chế \(Cl_2\) : Điện phân dung dịch KC1 trong nước, có màng ngăn. Điều chế \(Br_2\) : Cho \(H_2SO_4\) đặc tác dụng với hỗn hợp rắn là KBr và \(MnO_2\), đun nóng. Các phản ứng xảy ra như sau :
Phản ứng tổng của (1), (2), (3) là : \(2KBr + MnO_2 + 2H_2SO_4 \buildrel {{t^o}} \over \longrightarrow K2SO_4 + MnSO_4 + Br_2 + 2H_2O\) (4) Điều chế \(I_2\) tương tự điểu chế \(Br_2\) và có phản ứng tổng là : \(2KI + MnO_2 + 2H_2SO_4 \buildrel {{t^o}} \over \longrightarrow K2SO_4 + MnSO_4 + I_2 + 2H_2O\) - Điều chế các hiđro halogenua từ các muối tương ứng : - Điều chế HF : \(KF + H_2SO_4\buildrel {{t^o}} \over \longrightarrow KHSO_4 + HF↑\) - Điều chế HCL : \(KCl + H_2SO_4\buildrel {{t^o}} \over \longrightarrow KHSO_4 + HCl↑\) Điều chế HBr : Điện phân dung dịch KBr có màng ngăn (hoặc cho \(Cl_2\) tác dụng với dung dịch KBr, hoặc cho muối KBr tác dụng với hỗn hợp \(MnO_2\) và \(H_2SO_4\) đặc) được \(Br_2\), sau đó cho \(Br_2\) tác dụng với \(H_2\) ở nhiệt độ cao được HBr. \(H_2 + Br_2 \buildrel {{t^o}} \over \longrightarrow 2HBr\) Điều chế HI : Tương tự như điều chế HBr ở trên hoặc từ \(I_2\) ta điều chế HI bằng cách dùng khí \(H_2S\) khử \(I_2\). \(I_2 + H_2S \buildrel {{t^o}} \over \longrightarrow 2HI + S↓\) Sachbaitap.com
Xem lời giải SGK - Hóa 10 - Xem ngay >> 2K11 học trực tuyến Lớp 10 cùng thầy cô giáo giỏi tại Tuyensinh247.com, Kiến thức cập nhật theo chương trình mới nhất. Cam kết giúp học sinh học tốt, bứt phá điểm 9,10 chỉ sau 3 tháng, hoàn trả học phí nếu học không hiệu quả.
Xem thêm tại đây:
BÀI 26. LUYỆN TẬP: NHÓM HALOGEN
|
-
Bài 5.73 trang 56 Sách bài tập (SBT) Hóa học 10
Tính khối lượng muối NaCl và muối NaI cần thiết để có 10 tấn muối ăn chứa 2,5% NaI.
-

Bài 5.74 trang 56 Sách bài tập (SBT) Hóa học 10
Cho các chất sau : KC1, CaCl2, MnO2, dung dịch H2SO4) đặc. Đem trộn 2 hoặc 3 chất với nhau. Trộn như thế nào thì tạo thành clo ? Trộn như thế nào thì tạo thành hiđro clorua ? Viết PTHH của các phản ứng.
-
Bài 5.75 trang 56 Sách bài tập (SBT) Hóa học 10
Dựa vào cấu tạo, hãy giải thích vì sao tính oxi hoá của ion hipoclorit (ClO^-) mạnh hơn ion clorat (ClO_3^-). Lấy thí dụ phản ứng để minh hoạ.
-
Bài 5.76 trang 57 Sách bài tập (SBT) Hóa học 10
Khi đun nóng muối kaliclorat, không có xúc tác, thì muối này bị phân huỷ đồng thời theo 2 phản ứng sau :

 Tải ngay
Tải ngay