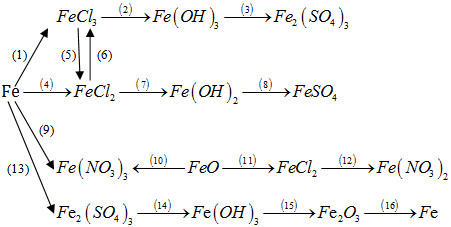Bài 7.113 trang 92 sách bài tập (SBT) Hóa học 12Thực hiện những biến đổi hoá học trong sơ đồ sau bằng cách viết phương trình hoá học của các phản ứng và nêu điều kiện của phản ứng (nếu có). Thực hiện những biến đổi hoá học trong sơ đồ sau bằng cách viết phương trình hoá học của các phản ứng và nêu điều kiện của phản ứng (nếu có).
Hướng dẫn trả lời: \(\left( 1 \right){\rm{ }}2Fe + {\rm{ }}3C{l_2}\buildrel {{t^0}} \over (2) FeCl3 + 3NaOH → Fe(OH)3 + 3NaCl (3) 2Fe(OH)3 + 3H2SO4 → Fe2(SO4)3 + 3H2O (4) Fe + 2HCl → FeCl2 + H2 (5) 2FeCl3 + Fe → 3FeCl2 (6) 2FeCl2 + Cl2 → 2FeCl3 (7) FeCl2 + 2NaOH → Fe(OH)2 + 2NaCl (8) Fe(OH)2 + H2SO4 → FeSO4 + 2H2O (9) Fe + 4HNO3 → Fe(NO3)3 + NO + 2H2O (10) FeO + 4HNO3 → Fe(NO3)3 + NO2 + 2H2O (11) FeO + 2HCl → FeCl2 + H2O (12) FeCl2 + 2AgNO3→ Fe(NO3)2 + 2AgCl↓ (13) 2Fe + 6H2SO4 (đ) → Fe2(SO4)3 + 3SO2 +6H2O (14) Fe2(SO4)3 + 6NaOH → 2Fe(OH)3↓ + 3Na2SO4 \(\eqalign{ Sachbaitap.com
Xem lời giải SGK - Hóa 12 - Xem ngay >> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
Xem thêm tại đây:
Bài 37. Luyện tập. TÍNH CHẤT HÓA HỌC CỦA SÁT VÀ HỢP CHẤT CỦA SẮT
|
-

Bài 7.114 trang 92 sách bài tập (SBT) Hóa học 12
Dung dịch A có chứa CuSO4 và Fe2(S04)3 a) Thêm Mg vào dung dịch A→ dung dịch B có 3 muối tan.
-

Bài 7.115 trang 92 sách bài tập (SBT) Hóa học 12
Nhận biết từng oxit kim loại riêng biệt sau bằng phương pháp hoá học : CuO, Al2O3, FeO, Fe3O4, Fe2O3, CaO. Giải thích và viết phương trình hoá học của các phản ứng
-

Bài 7.116 trang 92 sách bài tập (SBT) Hóa học 12
Muốn có đủ khí clo để tác dụng với 1,12 g Fe cần phải dùng bao nhiêu gam K2Cr2O7 và bao nhiêu mililít dung dịch HCl 36,5% (D = 1,19 g/ml)
-

Bài 7.117 trang 92 sách bài tập (SBT) Hóa học 12
Hỗn hợp A gồm Fe và kim loại M có hoá trị không đổi trong mọi hợp chất, M đứng trước hiđro trong dãy điện hoá. Tỉ lệ số mol của M và Fe trong hỗn hợp A là 1 : 2.

 Tải ngay
Tải ngay