Bài tập trắc nghiệm 3.1, 3.2, 3.3, 3.4, 3.5, 3.6 trang 27 Sách bài tập ( SBT) Hóa học 103.2.Cấu hình electron nguyên tử X và Y lần lượt là (1s^22s^22p^63s^23p^64s^1) và (1s^22s^22p^5) Liên kết hoá học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết 3.1.Các ion và nguyên tử 9F-, 10Ne, 11Na+ giống nhau về A. số khối. B. số electron. C. số proton. D. số nơtron 3.2.Cấu hình electron nguyên tử X và Y lần lượt là 1s22s22p63s23p64s1 và 1s22s22p5 Liên kết hoá học giữa nguyên tử X và nguyên tử Y thuộc loại liên kết A. cho - nhận. B. kim loại. C. ion D. cộng hoá trị. 3.3. X thuộc chu kì 3, nhóm IA, Y thuộc chu kì 3, nhóm VIIA. Công thức phân tử và bản chất liên kết của hợp chất giữa X và Y là A. X2Y ; liên kết ion B. XY ; liên kết ion. C. XY2 ; liên kết cộng hoá trị. D. X2Y2 ; liên kết cộng hoá trị. 3.4. Hợp chất trong phân tử có liên kết ion là A. NH4Cl. B.NH3. C. HCl. D.H2O. 3.5. Khi phản ứng hoá học xảy ra giữa những nguyên tử có cấu hình electron ở trạng thái cơ bản là 1s22s1 và 1s22s22p5 thì liên kết này là A. liên kết cộng hoá trị có cực . B. liên kết cộng hoá trị không cực C. liên kết ion D. liên kết kim loại 3.6. Cấu hình electron nguyên tử A là [Ar]4s2 và nguyên tử B là [Ne]3s23p5. Công thức hợp chất giữa A và B và bản chất liên kết trong hợp này là A. AB2, ion. B. AB, ion. C. A2B , cộng hoá trị. D.A2B3, kim loại. ĐÁP ÁN:
Sachbaitap.com
Xem lời giải SGK - Hóa 10 - Xem ngay >> 2K11 học trực tuyến Lớp 10 cùng thầy cô giáo giỏi tại Tuyensinh247.com, Kiến thức cập nhật theo chương trình mới nhất. Cam kết giúp học sinh học tốt, bứt phá điểm 9,10 chỉ sau 3 tháng, hoàn trả học phí nếu học không hiệu quả.
Xem thêm tại đây:
BÀI 12. LIÊN KẾT ION - TINH THỂ ION
|
-
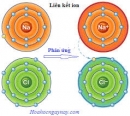
Bài 3.7 trang 27 Sách bài tập (SBT) Hóa học 10
Điện tích của electron và điện tích của proton (tính ra culông, C) bằng bao nhiêu ? Hãy cho biết tên gọi và kí hiệu của các điện tích đó ?
-
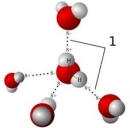
Bài 3.8 trang 27 Sách bài tập (SBT) Hóa học 10
a) Hãy cho biết quan hệ giữa số proton và số electron trong nguyên tử. Tại sao nguyên tử lại trung hoà điện ? b)Khi nguyên tử nhận thêm hay nhường đi một số electron thì phần tử còn lại có mang điện tích không và được gọi là gì ?
-

Bài 3.9 trang 27 Sách bài tập (SBT) Hóa học 10
Nguyên tử liti (Z = 3) có bao nhiêu proton, bao nhiêu electron ? Khi nhường đi một electron thì ion được hình thành mang điện tích dương hay âm ? lon đó thuộc loại ion gì ? Cho biết tên của ion đó.
-

Bài 3.10 trang 27 Sách bài tập (SBT) Hóa học 10
Nguyên tử fio (Z = 9) có bao nhiêu proton, bao nhiêu electron ? Khi nhận thêm một electron thì ion được hình thành mang điện tích dương hay âm ? lon đó thuộc loại ion gì ? Cho biết tên của ion đó.

 Tải ngay
Tải ngay







