Câu 6.14 trang 50 Sách bài tập (SBT) Hoá Nâng caoHãy xác định khối lượng của mỗi muối trong hỗn hợp. Cho 2,464 lít \(C{O_2}\) (đktc) đi qua dung dịch NaOH, người ta thu được 11,44 g hỗn hợp hai muối \(N{a_2}C{O_3}\) và \(NaHC{O_3}\). Hãy xác định khối lượng của mỗi muối trong hỗn hợp. Đáp án \(2NaOH + C{O_2} \to N{a_2}C{O_3} + {H_2}O\) (1) x mol x mol \(NaOH + C{O_2} \to NaHC{O_3}\) (2) y mol y mol \({n_{C{O_2}}} = {{2,464} \over {22,4}} = 0,11\left( {mol} \right)\) Gọi x, y là số mol \(N{a_2}C{O_3}\) và \(NaHC{O_3}\) Theo đề bài ra, ta có hệ phương trình: \(\left\{ \matrix{ x + y = 0,11 \hfill \cr 106x + 84y = 11,44 \hfill \cr} \right. \Rightarrow \left\{ \matrix{ x = 0,1 \hfill \cr y = 0,01 \hfill \cr} \right.\) \( \Rightarrow \)Hỗn hợp muối sinh ra có: 10,6 g \(N{a_2}C{O_3}\) và 0,84 g \(NaHC{O_3}\). Sachbaitap.com
Xem lời giải SGK - Hóa 12 Nâng cao - Xem ngay >> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
Xem thêm tại đây:
Bài 29. Một số hợp chất quan trọng của kim loại kiềm
|
-
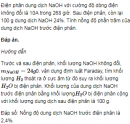
Câu 6.15 trang 50 Sách bài tập (SBT) Hóa Nâng cao
Tính nồng độ phần trăm của dung dịch NaOH trước điện phân.
-

Câu 6.16 trang 50 Sách bài tập (SBT) Hóa Nâng cao
Nhận định đúng khi nói về nhóm kim loại kiềm thổ và các nhóm kim loại thuộc nhóm A nói chung là:
-
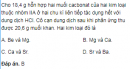
Câu 6.17 trang 50 Sách bài tập (SBT) Hóa Nâng cao
Cho 18,4 g hỗn hợp hai muối cacbonat của hai kim loại thuộc nhóm IIA ở hai chu kì liên tiếp tác dụng hết với dung dịch HCl. Cô cạn dung dịch sau khi phản ứng thu được 20,6 g muối khan. Hai kim loại đó là
-

Câu 6.19 trang 51 Sách bài tập (SBT) Hóa Nâng cao
Nhóm IIA gồm những nguyên tố: Be, Mg, Ca, Sr, Ba, Ra (nguyên tố phóng xạ).

 Tải ngay
Tải ngay







