-
Bài 2.51 , 2.52, 2.53 trang 23 Sách bài tập (SBT) Hóa học 10
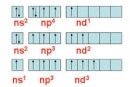
2.51. Trong bảng tuần hoàn các nguyên tố, nhóm gồm những nguyên tố kim loại điển hình là nhóm A.IIIA. B. VA. C. VIIA. D.IA.
-
Bài 2.58 trang 24 Sách bài tập (SBT) Hóa học 10
Nguyên tố X có hoá trị cao nhất trong oxit là a và hoá trị trong hợp chất khí với hiđro là b. Nêu mối quan hệ giữa a và b.
-

Bài 2.54 trang 23 Sách bài tập (SBT) Hóa học 10
Nguyên tử X có số thứ tự là 20, thuộc chu kì 4, nhóm IIA. Hãy cho biết số proton, số electron trong một nguyên tử X. Hãy viết cấu hình electron của nguyên tử X.
-

Bài 2.55 trang 23 Sách bài tập (SBT) Hóa học 10
Nguyên tố X có cấu hình electron nguyên tử : (1s^2 2s^2 2p^6 3s^2 3p^6). a) Hãy cho biết số proton có trong nguyên tử, số thứ tự của nguyên tố trong bảng tuần hoàn. b) Hãy cho biết số lớp electron và số electron ở lớp ngoài cùng.
-

Bài 2.56 trang 23 Sách bài tập (SBT) Hóa học 10
a) Hãy so sánh tính kim loại của magie (Mg), Z = 12, với nguyên tố đứng trước : natri (Na), Z = 11, và nguyên tố đứng sau : nhôm (Al), Z = 13. Hãy so sánh tính kim loại của magie (Mg), Z = 12, với nguyên tố đứng trên (trong cùng một nhóm) : beri (Be), Z = 4, và nguyên tố đứng dưới : canxi (Ca), Z = 20.
-

Bài 2.57 trang 23 Sách bài tập (SBT) Hóa học 10
Nguyên tố X hoá hợp với H cho hợp chất XH4. Oxit cao nhất của nó chứa 53,3% oxi về khối lượng. Tính số khối của X (coi số khối trùng với nguyên tử khối). X là nguyên tố nào ?
-

Bài 2.59 trang 24 Sách bài tập (SBT) Hóa học 10
Oxit cao nhất của nguyên tố R có công thức là R2O5 (A). Trong hợp chất với hiđro (B), R chiếm 82,35% về khối lượng. Xác định nguyên tố R và các công thức A, B.
-

Bài 2.60 trang 24 Sách bài tập (SBT) Hóa học 10
Nguyên tố Y thuộc nhóm VIA, oxit cao nhất của Y là A, hợp chất khí của Y với hiđro là B. Tỉ khối của B so với A là 0,425. Tìm Y, A, B.
-
Bài 2.61 trang 24 Sách bài tập (SBT) Hóa học 10
Cấu hình electron nguyên tử nguyên tố X là [Ne] (3s^23p^1) Cho biết vị trí (số thứ tự, chu kì, nhóm) của nguyên tố X trong bảng tuần hoàn. X là kim loại, phi kim hay khí hiếm ?
-
Bài 2.62 trang 24 Sách bài tập (SBT) Hóa học 10
Cho 0,64 g hỗn hợp hai kim loại X, Y (cùng thuộc nhóm IIA và ở hai chu kì kế tiếp) tác dụng với dung dịch HC1 dư, thu được 448 ml H2 (đktc). Xác định hai kim loại.

 Tải ngay
Tải ngay