Bài 38.13 Trang 54 Sách bài tập (SBT) Hóa học 8Xác định hoá trị của Ca, Na, Fe, Cu, AI trong các hiđroxit sau đây : Ca(OH)2, NaOH, Fe(OH)3, Cu(OH)2, Al(OH)3. a) Xác định hoá trị của Ca, Na, Fe, Cu, AI trong các hiđroxit sau đây : Ca(OH)2, NaOH, Fe(OH)3, Cu(OH)2, Al(OH)3. b) Cho 1,35 g nhôm tác dụng với dung dịch chứa 7,3 g HCl. Khối lượng muối tạo thành là A. 3,3375 g B. 6,675 g. C. 7,775 g. D. 10,775 g. Trả lời a) Trong phân tử bazơ, số nhóm OH bằng hoá trị của kim loại ; nhóm OH có hoá trị bằng I. Do đó trong : Ca(OH)2 : Ca có hoá trị II ; NaOH : Na có hoá trị I ; Fe(OH)3 : Fe có hoá trị III ; Cu(OH)2 : Cu hoá trị II ; Al(OH)3 : Al có hoá trị III b) Phương án B. Phương trình hoá học : \(2Al\,\,\,\,\,\,\, + \,\,\,\,\,\,\,\,6HCl\, \to 2AlC{l_3}\,\,\,\,\,\, + \,\,\,\,\,3{H_2} \uparrow \) 2 mol 6 mol 2 mol \({n_{Al}} = 0,05mol\) 0,05 mol 0,2 mol x mol \({n_{HCl}} = 0,2mol\) Theo phương trình trên, ta nhận thấy dư HCl, nên tính số mol AlCl3 theo số mol Al : \(x = 0,05mol \to {m_{AlC{l_3}}} = 0,05 \times 133,5 = 6,675(g)\)
Xem lời giải SGK - Hóa 8 - Xem ngay >> Học trực tuyến lớp 8 trên Tuyensinh247.com Học bám sát chương trình SGK mới nhất của Bộ Giáo dục. Cam kết giúp học sinh lớp 8 học tốt, hoàn trả học phí nếu học không hiệu quả. Phụ huynh và học sinh tham khảo chi tiết khoá học tại: Link
Xem thêm tại đây:
Bài 38: Luyện tập chương 5 - Hóa học 8
|
-

Bài 38.14 Trang 54 Sách bài tập (SBT) Hóa học 8
Hãy nêu phương pháp nhận biết các khí: cacbon đioxit, oxi, nitơ, hiđro
-
Bài 38.15 Trang 54 Sách bài tập (SBT) Hóa học 8
Cho 60,5 g hỗn hợp gồm hai kim loại kẽm Zn và sắt Fe tác dụng hết với dung dịch axit clohiđric. Thành phần phần trăm khối lượng của sắt trong hỗnl hợp là 46,289%. Tính :
-

Bài 38.16 Trang 54 Sách bài tập (SBT) Hóa học 8
Cho 22,4 g sắt tác dụng với dung dịch loãng có chứa 24,5 g axit H2SO4.
-
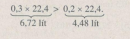
Bài 38.17 Trang 54 Sách bài tập (SBT) Hóa học 8
Dẫn 6,72 lít (ở đktc) hỗn hợp hai khí H2 và CO từ từ qua hỗn hợp hai oxit FeO và CuO nung nóng, sau phản ứng thấy khối lượng hỗn hợp giảm m gam.

 Tải ngay
Tải ngay





