Bài 44.2 Trang 60 Sách bài tập (SBT) Hóa học 8Có : CuSO4 và nước cất. Hãy tính toán và trình bày cách pha chế để có được những sản phẩm sau : Có : CuSO4 và nước cất. Hãy tính toán và trình bày cách pha chế để có được những sản phẩm sau : a) 50 ml dung dịch CuSO4 có nồng độ IM. b) 50 g dung dịch CuSO4 có nồng độ 10%. Trả lời a) Pha chế 50 ml dung dịch CuSO4 1M : - Số mol CuSO4 cần dùng là : \({n_{CuS{O_4}}} = {{1 \times 50} \over {1000}} = 0,05(mol)\, có khối lượng là: \({m_{CuS{O_4}}} = 160 \times 0,05 = 8(g)\) - Cách pha chế: Cân 8 g CuSO4 cho vào cốc chia độ. Thêm khoảng 25 - 30 ml nước cất vào cốc, dùng đũa thuỷ tinh khuấy cho CuSO4 tan hết, bỏ đũa ra ngoài, thêm từ từ nước cất cho đủ 50 ml. Trộn đều, ta được 50 ml dung dịch CuSO4 có nồng độ 1M. b) Pha chế 50 g dung dịch CuSO4 10% : - Khối lượng CuSO4 cần dùng là : \({m_{CuS{O_4}}} = {{10 \times 50} \over {100}} = 5(g)\) - Khối lượng nước cất cần dùng là : 50-5 = 45 (g) -Cách pha chế: Cân lấy 5 g CuSO4 cho vào cốc. Rót từ từ vào cốc 45 g hoặc 45 ml nước cất, khuấy cho CuSO4 tan hết, ta được 50 g dung dịch CuSO4 10%.
Xem lời giải SGK - Hóa 8 - Xem ngay >> Học trực tuyến lớp 8 trên Tuyensinh247.com Học bám sát chương trình SGK mới nhất của Bộ Giáo dục. Cam kết giúp học sinh lớp 8 học tốt, hoàn trả học phí nếu học không hiệu quả. Phụ huynh và học sinh tham khảo chi tiết khoá học tại: Link
Xem thêm tại đây:
Bài 44: Luyện tập chương 6 - Hóa học 8
|
-
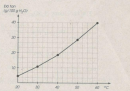
Bài 44.3 Trang 60 Sách bài tập (SBT) Hóa học 8
Bảng dưới đây cho biết độ tan của một muối trong nước thay đổi theo nhiệt độ :
-

Bài 44.4 Trang 60 Sách bài tập (SBT) Hóa học 8
Người ta pha chế một dung dịch NaCl ở 20°C bằng cách hoà tan 23,5 g NaCl trong 75 g nước. Căn cứ vào độ tan của NaCl
-
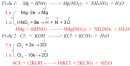
Bài 44.5 Trang 61 Sách bài tập (SBT) Hóa học 8
Hãy tính toán và trình bày cách pha chế 0,5 lít dung dịch H2SO4 có nồng độ 1M từ H2SO4 có nồng độ 98%, khối lượng riêng là 1,84 g/ml.
-

Bài 44.6* Trang 61 Sách bài tập (SBT) Hóa học 8
A là dung dịch H2SO4 có nồng độ 0,2M. B là dung dịch H2SO4 có nồng độ 0,5M.

 Tải ngay
Tải ngay





