Bài 5.63 trang 55 Sách bài tập (SBT) Hóa học 10Tính khử của HBr (ở trạng thái khí cũng như trong dung dịch) mạnh hơn HCL. Hãy lập PTHH của các phản ứng trong 2 trường hợp sau : Tính khử của HBr (ở trạng thái khí cũng như trong dung dịch) mạnh hơn HCL. Hãy lập PTHH của các phản ứng trong 2 trường hợp sau : a) HBr khử \(H_2SO_4\) đến \(SO_2\). b) Dung dịch HBr không màu, để lâu trong không khí trở nên có màu vàng nâu vì bị oxi hoá bởi \(O_2\) của không khí. Lời giải: a) \(2HBr + H_2SO_4 → Br_2 + SO_2 + 2H_2O\) b) \(4HBr + O_2 → 2Br_2 + 2H_2O\) Sachbaitap.com
Xem lời giải SGK - Hóa 10 - Xem ngay >> 2K11 học trực tuyến Lớp 10 cùng thầy cô giáo giỏi tại Tuyensinh247.com, Kiến thức cập nhật theo chương trình mới nhất. Cam kết giúp học sinh học tốt, bứt phá điểm 9,10 chỉ sau 3 tháng, hoàn trả học phí nếu học không hiệu quả.
Xem thêm tại đây:
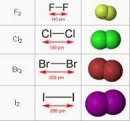
BÀI 25. FLO - BROM - IOT
|
-

Bài 5.64 trang 55 Sách bài tập (SBT) Hóa học 10
Muối MgCl2 bị lẫn một ít muối MgBr2. Tìm cách loại bỏ tạp chất để được muối MgCl2 tinh khiết.
-
Bài tập trắc nghiệm 5.65, 5.66, 5.67, 5.68, 5.69 trang 55 Sách bài tập (SBT) Hóa học 10
5.63.Cho phản ứng : SO2 + Br2 + 2H2O → H2SO4 + 2X)
-

Bài 5.70 trang 56 Sách bài tập (SBT) Hóa học 10
Vìsao người ta có thể điều chế (Cl2, Br2, I2) bằng cách cho hỗn hợp dung dịch (H2SO4) đặc và (MnO2) tác dụng với muối clorua, bromua, iotua nhưng không thể áp dụng phương pháp này để điều chế F2 ? Bằng cách nào có thể điều chế được F2 ? Viết PTHH của các phản ứng.
-
Bài 5.71 trang 56 Sách bài tập (SBT) Hóa học 10
Bằng phương pháp hoá học nào có thể a)Xác định được có khí clo lẫn trong khí hiđro clorua ? b)Thu được khí clo từ hỗn hợp khí ở câu a ?

 Tải ngay
Tải ngay







