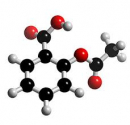
Bài tập 9.35 trang 70 sách bài tập(SBT) hóa học 11Hỗn hợp M chứa ba hợp chất hữu cơ X, Y và Z 9.33. Hỗn hợp M chứa ba hợp chất hữu cơ X, Y và Z. Hai chất X và Y kế tiếp nhau trong một dãy đồng đẳng ( \({M_Y} > {M_X}\) ). Chất Z là đồng phân của chất Y. Nếu làm bay hơi 3,2 g M thì thể tích hơi thu được đúng bằng thể tích của 1,68g khí nitơ ở cùng điều kiện. Để đốt cháy hoàn toàn 16g M cần dùng vừa hết 23,52 lít \({O_2}\) (đktc). Sản phẩm cháy chỉ có \(C{O_2}\) và \({H_2}O\) với số mol bằng nhau. Nếu cho 48g M tác dụng với Na(lấy dư), thu được 1,68 lít \({H_2}\)(đktc). Hãy xác địng công thức phân tử, công thức cấu tạo, tên và phần trăm về khối lượng của từng chất trong hỗn hợp M. Hướng dẫn trả lời: Số mol 3 chất trong 3,20 g hỗn hợp M : \(\frac{{1,68}}{{28}}\) = 0,06 (mol). Số mol 3 chất trong 16 g M : \(\frac{{0,06.16}}{{3,2}}\) = 0,3 (mol) Khi đốt hỗn hợp M ta chỉ thu được C02 và H20. Vậy, các chất trong hỗn hợp đó chỉ có thể chứa C, H và O. Đặt công thức chất X là CxHyOz thì chất Y là Cx+1Hy+2Oz.Chất Z là đồng phân của Y nên công thức phân tử giống chất Y. Giả sử trong 16 g hỗn hợp M có a mol chất X và b mol hai chất Y và Z : \(\left\{ \begin{array}{l} Khi đốt 16 g M thì tổng khối lượng C02 và H20 thu được bằng tổng khối lượng của M và 02 và bằng : \(16 + \frac{{23,52}}{{22,4}}.32 = 49,6(g)\) Mặt khác, số mol C02 = số mol H20 = n : 44n + 18n = 49,6 \( \Rightarrow \) n = 0,8 \({C_x}{H_y}{O_z} + (x + \frac{y}{4} - \frac{z}{2}){O_2} \to xC{O_2} + \frac{y}{2}{H_2}O\) a mol xa mol \(\frac{y}{2}\)a mol \({C_{x + 1}}{H_{y + 2}}{O_z} + (x + \frac{y}{4} - \frac{z}{2} + 1,5){O_2}\)\( \to (x + 1)C{O_2} + \frac{{y + 2}}{2}{H_2}O\) b mol (x + 1)b mol \(\frac{{y + 2}}{2}\)b mol Số mol C02 là : xa + (x + 1)b = 0,8 (mol) (3) Số mol H20 là : \(\frac{{y{\rm{a}} + (y + 2)b}}{2}\) = 0,8 (mol) do đó : ya + (y + 2)b = 1,6 (4) Giải hệ phương trình : Biến đổi (3) ta có x(a + b) + b = 0,8 Vì a + b = 0,3 nên b = 0,8 - 0,3x Vì 0 < b < 0,3 nên 0 < 0,8 - 0,3x < 0,3 \( \Rightarrow \) 1,66 < x < 2,66 x nguyên \( \Rightarrow \) x = 2 \( \Rightarrow \) b = 0,8 - 0,3.2 = 0,2 \( \Rightarrow \) a = 0,3 - 0,2 = 0,1 Thay giá trị của a và b vào (4), tìm được y = 4. Thay giá trị của a, b, x và y vào (2), tìm được z = 1. Vậy chất X có CTPT là C2H40, hai chất Y và z có cùng CTPT là C3H60. Chất X chỉ có thể có CTCT là Chất Y là đồng đẳng của X nên CTCT là Hỗn hợp M có phản ứng với Na. Vậy, chất Z phải là ancol CH2 = CH - CH2 - OH (propenol) : 2CH2 = CH - CH2 - OH + 2Na \( \to \) 2CH2 = CH - CH2 - ONa + H2\( \uparrow \) Số mol Z trong 48 g M là : 2.số mol H2 = 2.\(\frac{{1,68}}{{22,4}}\) =0,15 (mol). Số mol z trong 16 g M là : \(\frac{{0,15.16}}{{48}}\) = 0,05 (mol) Số mol Y trong 16 g M là : 0,2 - 0,05 = 0,15 (mol). Thành phần khối lượng của hỗn hợp M : Chất X chiếm : \(\frac{{0,1.44}}{{16}}\). 100% = 27,5%. Chất Y chiếm : \(\frac{{0,15.58}}{{16}}\). 100% = 54,4%. Chất Z chiếm : \(\frac{{0,05.58}}{{16}}\). 100% = 18,1%. Sachbaitap.com
Xem lời giải SGK - Hóa 11 - Xem ngay >> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
Xem thêm tại đây:
Bài 46: Luyện tập: Anđehit - Xeton - Axit Cacboxylic
|
-
Bài tập 9.36 trang 70 sách bài tập(SBT) hóa học 11
Viết phương trình hoá học thưc hiện các biến hoá dưới đây
-

Bài tập 9.32 trang 70 sách bài tập(SBT) hóa học 11
Anđehit axetic có thể khử được đồng(II) hiđroxit trong môi trường kiềm

 Tải ngay
Tải ngay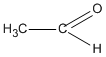 (etanal) vì chất CH2 = CH - OH không bền và chuyển ngay thành etanal.
(etanal) vì chất CH2 = CH - OH không bền và chuyển ngay thành etanal.