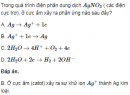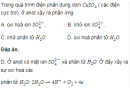Câu 5.34 trang 40 Sách bài tập (SBT) Hóa Nâng caoXác định kim loại mang đốt. Một bình kín dung tích 5 lít chứa oxi dưới áp suất 1,4 atm ở 27oC. Người ta đốt cháy hoàn toàn 12 g một kim loại hoá trị II ở bình đó. Sau phản ứng nhiệt độ trong bình là 136,5oC, áp suất là 0,903 atm, thể tích bình không đổi, thể tích chất rắn không đáng kể. Xác định kim loại mang đốt. Đáp án Gọi \({V_0}\) là thể tích ở đktc của lượng oxi trong bình trước phản ứng, \(V_0'\) là thể tích ở đktc của lượng oxi trong bình sau phản ứng. Ta có: \({{1.{V_0}} \over {273}} = {{1,4.5} \over {273 + 27}} \Rightarrow {V_0} = 6,37\) lít. \({{1.V_0'} \over {273}} = {{0,903.5} \over {273 + 136,5}} \Rightarrow V_0' = 3,01\) lít. Thể tích ở đktc của lượng oxi đã phản ứng: \({V_0} - V_0' = 6,37 - 3,01 = 3,36\)(lít) \(2M + {O_2} \to 2MO\) (1) Theo (1) , n kim loại = \(2{n_{{O_2}}} = 2.{{3,36} \over {22,4}} = 0,3\)(mol) Khối lượng mol của kim loại M là \({{12} \over {0,3}} = 40\left( {g/mol} \right) \) \(\Rightarrow \) Kim loại là Ca. Sachbaitap.com
Xem lời giải SGK - Hóa 12 Nâng cao - Xem ngay >> 2K9 Chú ý! Lộ Trình Sun 2027 - 1 lộ trình ôn đa kỳ thi (TN THPT, ĐGNL (Hà Nội/ Hồ Chí Minh), ĐGNL Sư Phạm, ĐGTD, ĐGNL Bộ Công an, ĐGNL Bộ Quốc phòngTD - Click xem ngay) tại Tuyensinh247.com. Cập nhật bám sát bộ SGK mới, Thầy Cô giáo giỏi, 3 bước chi tiết: Nền tảng lớp 12; Luyện thi chuyên sâu; Luyện đề đủ dạng đáp ứng mọi kì thi.
Xem thêm tại đây:
Bài 21. Luyện tập: Tính chất của kim loại
|
-
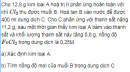
Câu 5.35 trang 40 Sách bài tập (SBT) Hóa Nâng cao
Xác định kim loại A. Tính nồng độ mol của muối B trong dung dịch C.
-

Câu 5.36 trang 40 Sách bài tập (SBT) Hóa Nâng cao
Trong quá trình điện phân, những ion âm(anion) di chuyển về

 Tải ngay
Tải ngay